Energi ini diukur pada titik didih zat dan walaupun nilainya biasanya dikoreksi ke 298 k koreksi ini kecil. Cara menentukan dan menghitung perubahan entalpi h rumus energi reaksi contoh soal pembahasan praktikum kimia perubahan δh reaksi dapat ditentukan dengan beberapa cara yakni dari hasil eksperimen dari penerapan hukum hess atau dengan data entalpi pembentukan dan energi ikatan.

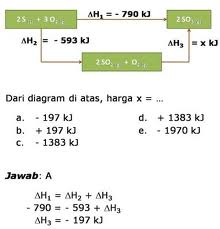
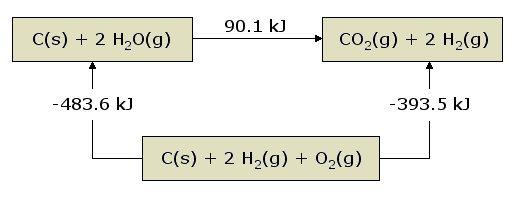
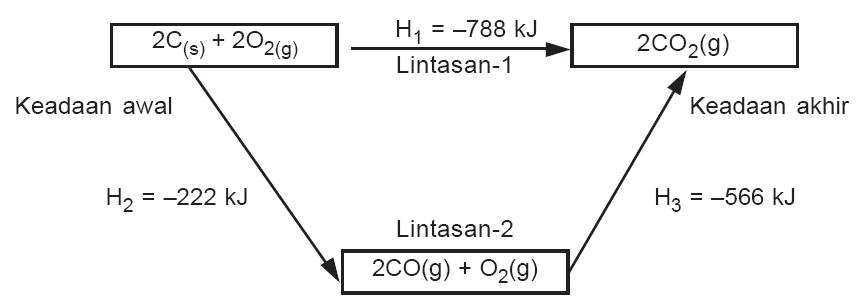
Contoh Soal Hukum Hess Bentuk Bagan
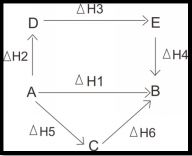
Contoh soal perubahan entalpi. Karena disini akan mengulas tentang pengertian termokimia sistem termokimia dan rumus termokimia beserta contohnya secara lengkap. Panas atau kalor penguapan atau lengkapnya perubahan entalpi penguapan standar δ v h o adalah energi yang dibutuhkan untuk mengubah suatu kuantitas zat menjadi gas. Entalpi tidak bergantung pada jalannya reaksi atau jumlah tahapan reaksi. Contoh soal berikut merupakan penjelasan tentang perubahan entalpi reaksi yang hanya tergantung pada keadaan awal dan akhir. Menentukan h reaksi bila perubahan entalpi pereaksi dan hasil reaksi diketahui menentukan h reaksi berdasarkan reaksi bersusun menentukan h reaksi dengan menganalisis diagram atau siklus reaksi yang. Beberapa model soal yang sering muncul untuk menghitung perubahan entalpi reaksi dengan hukum hess antara lain.
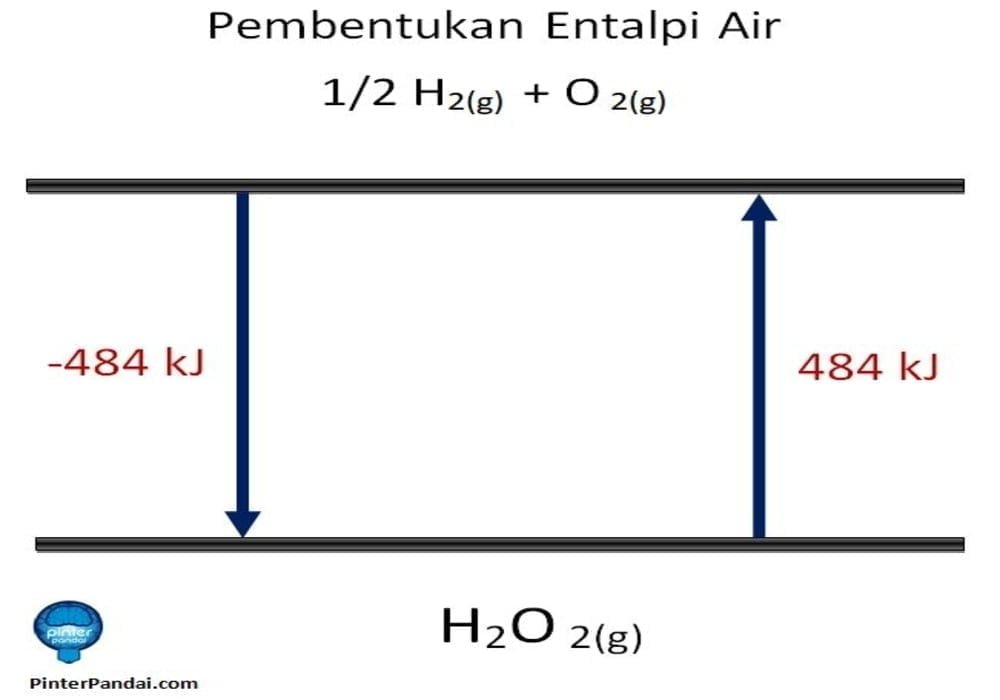
Contoh soal perhitungan perubahan entalpi reaksi pembakaran. Hukum hess digunakan untuk menentukan perubahan entalpi suatu reaksi. Entalpi penguapan adalah energi yang di butuhkan untuk mengubah suatu kuantitas zat menjadi gas. Diantaranya perubahan entalpi pembentukan standar δh 0 f. Ada beberapa jenis perubahan entalpi standar berdasarkan jenis reaksi kimia yang terjadi pada wujud zat. Pengertian persamaan reaksi rumus dan contoh soal tahukah anda apa yang dimaksud dengan termokimia.
Perubahan entalpi δh 0 dipengaruhi suhu dan tekanan yang diukur pada kondisi standarkondisi standar yaitu pada tekanan 1 atm dan suhu 25 0 c atau 298 k dengan satuan kj sedangkan satuan δh molar reaksi adalah kjmol.