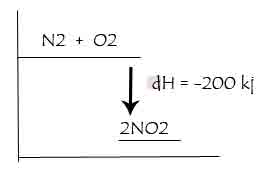
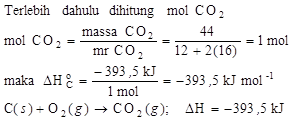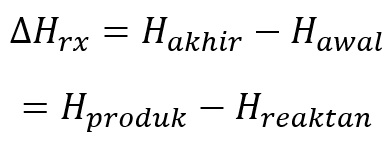1 mol gas hidrogen bereaksi dengan ½ mol gas oksigen menghasilkan air dengan melepaskan kalor sebesar 2855 kj. Persamaan termokimia reaksi pembentukan h20.
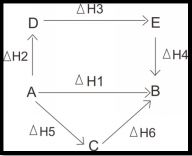
Termokimia Pengertian Rumus Contoh Soal
Contoh soal persamaan termokimia. Posted in kimia tagged contoh soal entalpi termodinamika contoh soal hukum hess contoh soal termokimia energi ikatan entalpi ikatan adalah entalpi pembentukan entalpi penguraian standar entalpi standar adalah grafik entalpi reaksi hubungan kalor dan entalpi kalorimeter kimia makalah termokimia materi termokimia pdf pengertian entalpi persamaan termokimia pertanyaan tentang. Soal termokimia pilihan ganda dan pembahasannya. Didalam persamaan termokimia. Data energi ikatan. H2o l h2g ½ o2g δh 286 kj. Ah f h 2 0ℓ 28585 kjmol.
Contoh soal reaksi eksoterm dan endoterm. Persamaan reaksi yang menunjukkan informasi d h. 31 45 contoh soal termokimia kelas 11 sma. Tuliskan persamaan termokimia untuk pembentukan satu mol air. Jadi pasangan persamaan reaksi yang merupakan reaksi pembentukan penguraian dan pembakaran sesuai dengan opsi yang ada adalah nomor 1 2 dan 4 d. Pengertian persamaan reaksi rumus dan contoh soal tahukah anda apa yang dimaksud dengan termokimia.
Persamaan termokimia dan entalpi. Berapakah kalor yang diperlukan untuk menguraikan 13 gram air menjadi hidrogen dan oksigen pada keadaan standar. Contoh soal dan jawaban persamaan termokimia. Persamaan termokimia entalpi pembentukan standar penguraian pembakaran netralisasi contoh soal pembahasan bagaimana cara menuliskan persamaan termokimiapenulisan reaksi persamaan termokimia mirip dengan penulisan reaksi biasa termasuk macam atom dan jumlah atomnya. Contoh soal tentang kalor. Unit pembangkit uap air di pabrik dinamakan.
Karena disini akan mengulas tentang pengertian termokimia sistem termokimia dan rumus termokimia beserta contohnya secara lengkap. 2h 2 g o 2 g 2h 2 og δh 4836 kj. C c 611 kjmol. Persamaan termokimia adalah persaman reaksi setara yang menyertakan kalor reaksi entalpi reaksi yang menunjukkan hubungan antara massa dan energi. Diketahui entalpi pembentukan standar h f h 2 0ℓ 28585 kjmol. H 2 g ½ o 2 g h 2 o l δh 2855 kj.
A r h 1 a r o 16 pembahasan. Pengertian rumus contoh soal march 26 2020 by eka termokimia merupakan cabang ilmu kimia yang mempelajari tentang panas atau kalor yang terdapat pada reaksi kimia maupun proses proses yang berhubungan dengan reaksi kimia. Tuliskan juga reaksi untuk kebalikannya. Persamaan reaksi nomor 1 tidak bisa dikatakan pembakaran n 2 karena koefisien n 2 tidak sama dengan 1. Pembentukan satu mol air berarti mengalikan persamaan termokimia dengan faktor ½ h2g ½ o2g h2o l δh 286 kj untuk reaksi kebalikannya. Perbedaannya h reaksi pada penulisan persamaan termokimia harus disertakan.