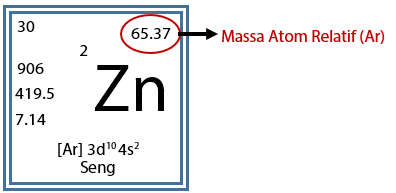
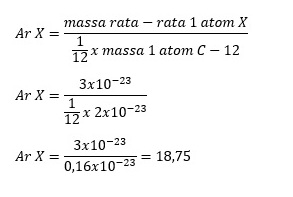Massa atom relatif tidak mempunyai satuan. Molaritas molalitas dan normalitas melibatkan massa molekul relatif dalam suatu larutan.

Hukum Dasar Kimia Dan Perhitungan Kimia
Contoh soal massa atom relatif. Nantinya massa atom relatif dan massa molekul relatif dapat digunakan dalam menentukan massa molar. Pemahaman tentang massa molekul relatif ini sangat berguna karena dalam materi materi lanjutan seperti topik konsentrasi dan larutan yang dinyatakan dengan. Materi tersebut akan dibahas lebih jauh pada materi konsep molsebelumnya simak cara menghitung massa atom relatif dan cara menghitung massa molekul relatif pada pembahasan di bawah. Contoh soal 1 massa atom relatif. Massa atom relatif x. Tutorial mata pelajaran kimia kita kali ini adalah bagaimana cara menghitung massa atom relatif dan juga massa molekul relatif.
Berapa massa atom relatif unsur x tersebut. Contoh soal dan pembahasan tentang massa atom relatif massa atom rata rata dan persentase massa massa unsur penyusun massa rata rata written by unknown published at 0651 categorized as kimia x soal pembahasan. Satuan sma tidak pernah dicantumkan dalam tabel periodik unsur. Massa atom relatif adalah perbandingan massa rata rata unsur x terhadap 112 x massa atom c 12 yang dirumuskan contoh soal no. Massa rata rata atom unsur x adalah 310 23 gr. And have 0 komentar.
Massa 1 atom c 12 12 sma atau 204 x 10 27kg tergantung apa yang ditanyakan apakah sma atau kg atau juga mungkin gram massa ratarata x merupakan massa ratarata dari semua isotop x yang ada di alam. Jika sobat melihat dalam tabel natrium memiliki nomor massa 23 maka artinya massa satu atom dari unsur natrium adalah 23 kali dari 112 massa atom c 12coba sobat hitung ingat lagi materi isotop isoton dan isobar. Sedangkan massa 1 atom c 12 adalah 210 23 gr. Di mana massa molar menyatakan massa yang dimiliki oleh 1 mol zat yang besarnya sama dengan ar atau mr. Jadi 112 massa atom c 12 112 x 1993 x 10 23 1661 x 10 24 g nilai 1 sma. Massa atom c 12 1993 x 10 23 g.