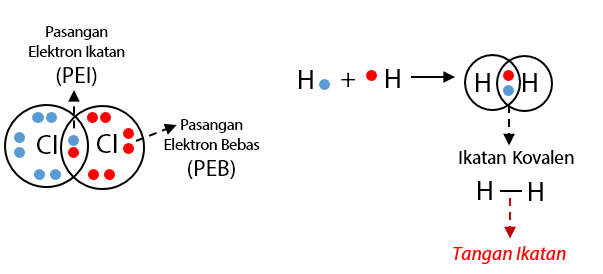
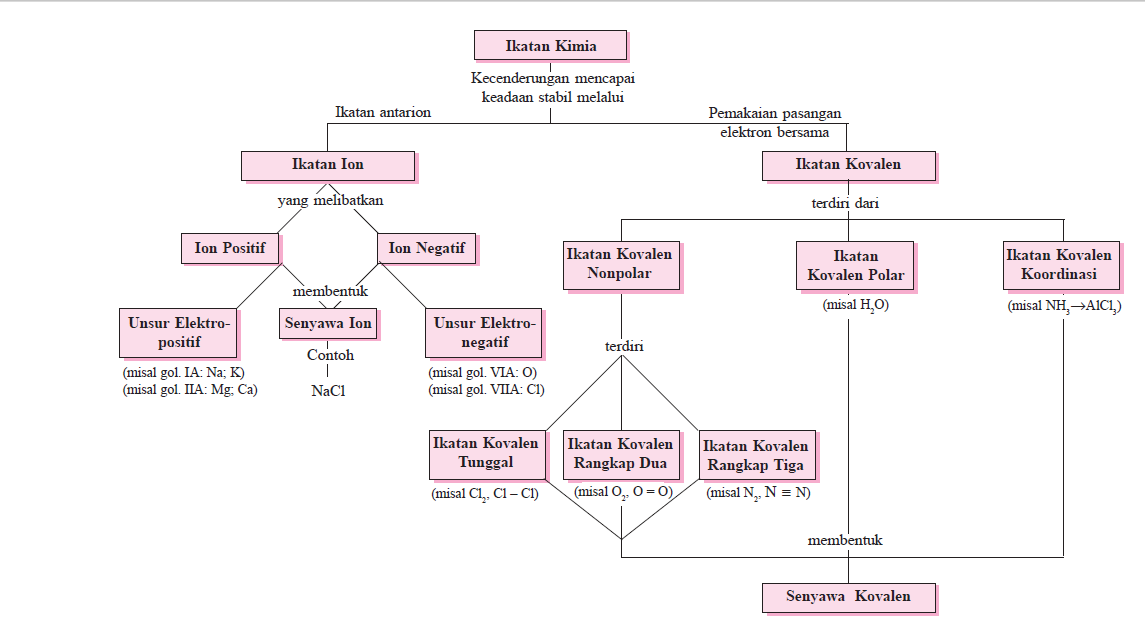
Tiap tiap ion na dikelilingi oleh ion cl sejumlah 6 ion. Senyawa ion merupakan senyawa yang terbentuk dari ikatan ionik yang terjadi antara dua unsur atau lebih.

Cara Membandingkan Karakter Ion Kovalen Senyawa Senyawa
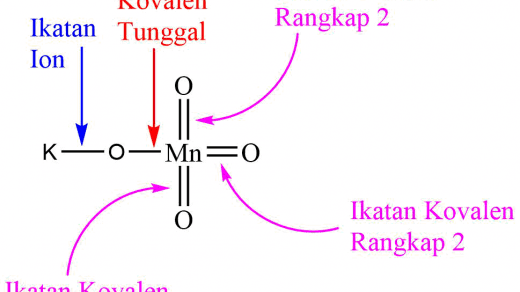
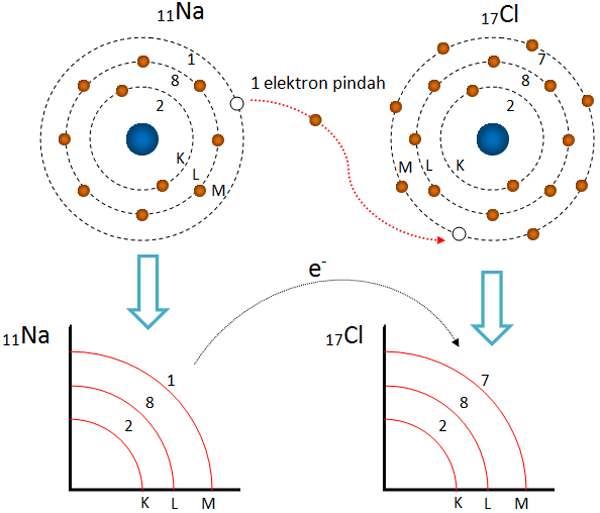
Contoh senyawa ikatan ion. Proses pembentukan ikatan ion antara k dan cl. Untuk membentuk senyawa ion terdapat syarat dan ketentuan yang harus dimiliki suatu unsur. Berikut mengenai syarat terjadinya ikatan ion. Senyawa ion adalah senyawa yang terbentuk dari ikatan ionik yang terjadi antara dua unsur atau lebih. Namun misalnya untuk senyawa kompleks feh 2 o 6 2 ion pusat fe 2 dengan molekul pengeliling h 2 o juga sebagian besar diikat oleh gaya gaya elektrostatik antara ion pusat dengan dipol listrik tetap yaitu negatif yang dihasilkan oleh molekul. Ikatan antara k dan cl 2 8 8 1 2 8 7.
Proses pembentukan ikatan ion antara li dan f. Contoh soal isotop isobar isoton. Hal ini terjadi akibat kuatnya ikatan antar molekul pada senyawa ion tersebut. Ikatan ion secara sederhana pengertian ikatan ion adalah ikatan antara dua macam ion kation dan anion oleh gaya gaya elektrostatik coulomb. Syarat terjadinya ikatan ion. Selain contoh contoh ikatan ion mungkin bermanfaat untuk mengetahui contoh contoh senyawa yang mengandung ikatan kovalen dan juga senyawa yang mengandung ikatan kimia ion dan kovalen.
Ikatan ion harus terjadi antara atom logam yang akan membentuk ion positif dengan atom non logam yang akan membentuk ion negatif hal ini dikarenakan agar timbul gaya tarik. Terimakasih atas kunjungannya dan sampai jumpa di artikel berikutnya. Contoh yang paling umum dari ikatan ion yaitu pembentukan natrium klorida di mana sebuah atom natrium menggabungkan dengan atom klorin. Demikianlah artikel tentang definisi ikatan ion proses pembentukan contoh senyawa ion serta sifat sifat senyawa ion. Beberapa sifat senyawa ion yaitu membentuk kristal namun rapuh titik lebur dan leleh nya tinggi mudah larut dalam air dan mampu menghantarkan listrik. Meskipun mereka terdiri dari ion bermuatan positif dan negatif senyawa ion netral secara elektrik karena muatannya selalu sama dan berlawanan.
Pada umumnya senyawa ionik merupakan gabungan antara unsur logam dan unsur nonlogam yang memiilki perbedaan keelektronegatifan yang tinggi. Selain menyebabkan tingginya titik didih dan titik beku dari senyawa ionkuatnya ikatan antar molekul ini juga berimbas pada sifat fase dari senyawa ion. Sebagai contoh senyawa nacl yang berbentuk kristal sebenarnya membentuk struktur kubus. 10 contoh larutan elektrolit dan non elektrolit dalam kehidupan sehari hari. Mari kita lihat pada konfigurasi elektronik masing masing. Pada umumnya senyawa ionik merupakan gabungan antara unsur logam dan unsur nonlogam yang memiilki perbedaan keelektronegatifan yang tinggi.
Senyawa ion umumnya memiliki titik didih dan titik beku yang cukup tinggi. Semoga dapat bermanfaat untuk anda. 281 dan klorin cl.